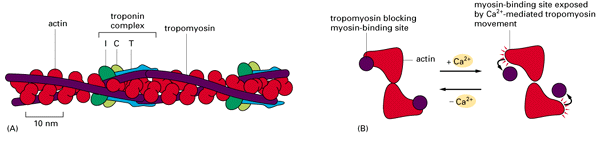
Os filamentos de actina e miosina tęm uma grande afinidade e ligam-se facilmente sem a presença do complexo troponina/tropomiosina. Nota-se que esse complexo impede a ligaçăo na ausęncia de Ca2+. O mecanismo de liberaçăo do sítio de ligaçăo actina/miosina começa com a chegada do potencial de açăo ŕ membrana do músculo, promovendo a entrada maciça de íons Ca2+ . Estes íons ligam-se ŕ troponina C, causando uma mudança conformacional da mesma que se reflete na molécula de tropomiosina, que libera entăo os sítios da actina que estavam bloqueados. A interaçăo actina/miosina se dá imediatamente desde que haja ATP e magnésio (ambos presentes em condiçőes normais).
